
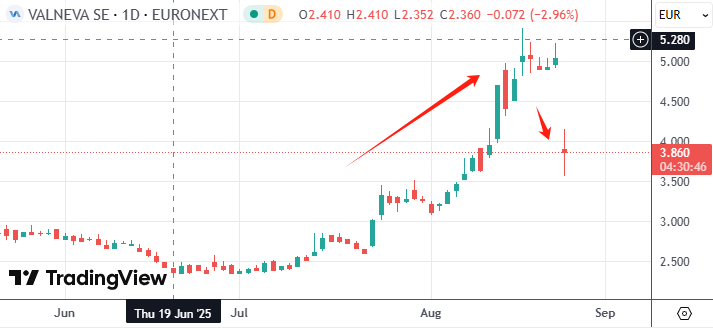
财联社8月25日讯(编辑 赵昊)周一(8月25日),在欧股交易的法国生物技术公司瓦尔内瓦(Valneva SE,欧股股票代码:VLA)股价跌超20%,因美国监管机构暂停了其基孔肯雅热疫苗的使用。
瓦尔内瓦在官网宣布,美国食品药品监督管理局(FDA)已暂停其基孔肯雅热疫苗“IXCHIQ”的许可证,理由是新增了4例严重不良事件,FDA周一要求瓦尔内瓦必须停止疫苗在美国的运输和销售。
分析指出,FDA最新的决定令市场非常意外,该股前三周均录得大涨,其中有两周累涨超20%。新闻稿提到,本月早些时候,美国FDA一度恢复了对老年人(大于等于60岁)的疫苗使用建议。
但在周一,FDA突然决定全面暂停该疫苗,因为在美国境外发生了4例严重不良事件:其中3例患者年龄在70至82岁之间(瓦尔内瓦强调有一名82岁患者住院两天后出院),另一例为55岁患者。
瓦尔内瓦表示,公司正在对严重不良事件案例进行详细调查,并将在必要时根据相关法律程序,就FDA的决定采取进一步措施。
瓦尔内瓦首席执行官Thomas Lingelbach写道,公司依然全力承诺确保疫苗的可及性,将继续向所有批准IXCHIQ的国家供应该疫苗。
财联社先前曾提到,目前美国市面上主要有两款基孔肯雅热疫苗,分别是瓦尔内瓦的IXCHIQ和巴伐利亚北欧的VIMKUNYA,其中IXCHIQ获批时间要较早一些,是首款通过FDA的疫苗。
瓦尔内瓦在新闻稿中提到,今年上半年,IXCHIQ为公司带来了750万欧元的销售额。公司正在评估若美国永久撤销许可证可能带来的财务影响,但目前并未调整其营收指引。

